

美国FDA规定从事医疗器械生产、制备、传播、合成、或加工的出口到美国的美国境外企业,需要向FDA指定一名美国代理人。
美国代理(必要条件)
1. 美国代理必须居住在美国或者在美国有一个商业场所;
2. 美国代理不仅仅只是接听服务,必须在正常的工作日可以保证或有职员接听FDA的电话。
美国代理的职责,包括但不限于:
1. 协助FDA与境外制造商沟通;
2. 协助境外制造商在进口产品或提供进口到美国时相应问题的回复;
3. 协助FDA对境外制造商的安排审厂;
4. 如果FDA不能直接或较快的联系到境外制造商,FDA会提供信息或文档给美国代理人,该行为被认为等同于向境外制造商提供了相同的信息或文档。




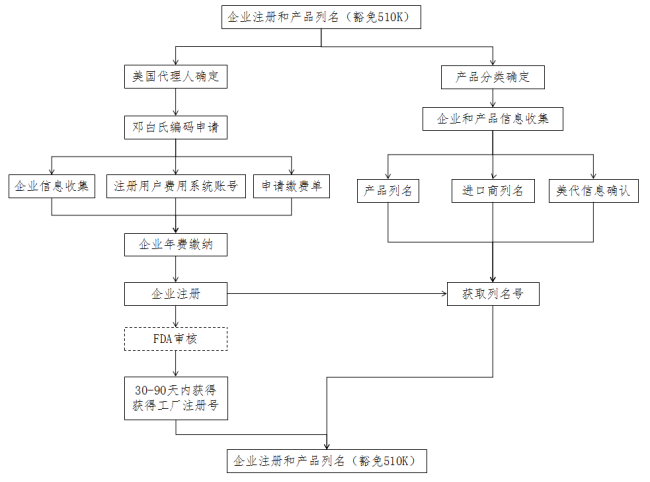
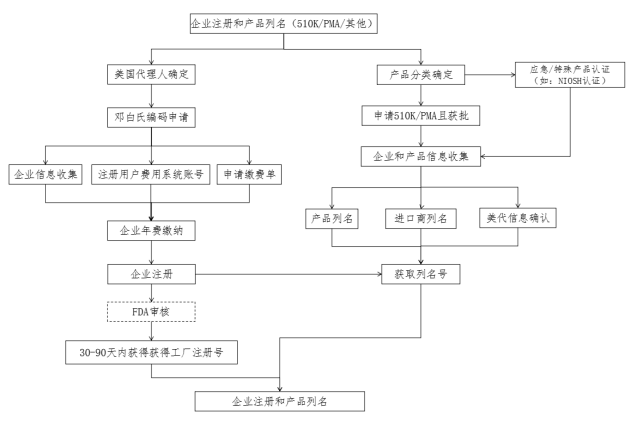
CFR - Code of Federal Regulations Title 21
PART 807 Establishment registration and device listing for manufacturers and initial importers of devices
官方费用
(2022财年)
项目 收费(美元) 产品列名 0 企业年费 5672
官方时间
审核内容 | FDA官方时间(天) |
产品列名 | 0 |
首次企业注册,注册号下发 | 90 |
参与到在美国进行商业流通的医疗器械的生产和销售的企业,都要求在FDA进行年度注册。以下表格列出了不同企业类型关于注册、列名及是否需要付年费的具体要求。
美国境内企业 | |||
活动 | 登记 | 列名 | 付费 |
合约制造商(包括合约包装商) | Yes | Yes | Yes |
合约灭菌商 | Yes | Yes | Yes |
器械正在开展IDE试验 | No | No | No |
不进口器械的国内分销商 | No | No | No |
设置在自由贸易区,并涉及生产、准备、宣传、组合、装配、加工器械并预期商业分销到美国的企业 | Yes | Yes | Yes |
非第一次拥有器械进口到美国的所有权的进口代理,经纪人及其他机构 | No | No | No |
初始进口商 | Yes | No | Yes |
抱怨文档持有者(21CFR 820.198)持有者 | Yes | Yes | Yes |
被包装或贴标后用于与健康相关商业分销给终端用户的配件或组件的生产商 | Yes | Yes | Yes |
仅分销给成品器械生产商的组件生产商 | No | No | No |
生产商(包括套装装配商Kit Assemblers) | Yes | Yes | Yes |
定制器械制造商 | Yes | Yes | Yes |
已经在美国商业销售的已用器械的再翻新商或再交易商 | No | No | No |
再贴标商或再包装商 | Yes | Yes | Yes |
再生产商 | Yes | Yes | Yes |
一次性器械的再加工商 | Yes | Yes | Yes |
仅进行规格咨询顾问 | No | No | No |
规格开发商 | Yes | Yes | Yes |
仅出口器械的美国制造商 | Yes | Yes | Yes |
不是生产商或进口商的批发商 | No | No | No |
美国境外企业 | |||
活动 | 登记 | 列名 | 付费 |
合约制造商(包括合约包装商) | Yes | Yes | Yes |
合约灭菌商 | Yes | Yes | Yes |
定制器械制造商 | Yes | Yes | Yes |
器械正在开展IDE试验 | No | No | No |
在美国境外的器械外国出口商 | Yes | Yes | Yes |
外国制造商(包括套装装配商Kit Assemblers) | Yes | Yes | Yes |
抱怨文档持有者(21CFR 820.198)持有者 | Yes | Yes | Yes |
被包装或贴标后用于与健康相关商业分销给终端用户的配件或组件的生产商 | Yes | Yes | Yes |
仅分销给成品器械生产商的组件生产商 | No | No | No |
再贴标商或再包装商 | Yes | Yes | Yes |
再生产商 | Yes | Yes | Yes |
一次性器械的再加工商 | Yes | Yes | Yes |
规格开发商 | Yes | Yes | Yes |