原文链接:
https://www.fda.gov/industry/fda-user-fee-programs/medical-device-user-fee-amendments-mdufa-fees
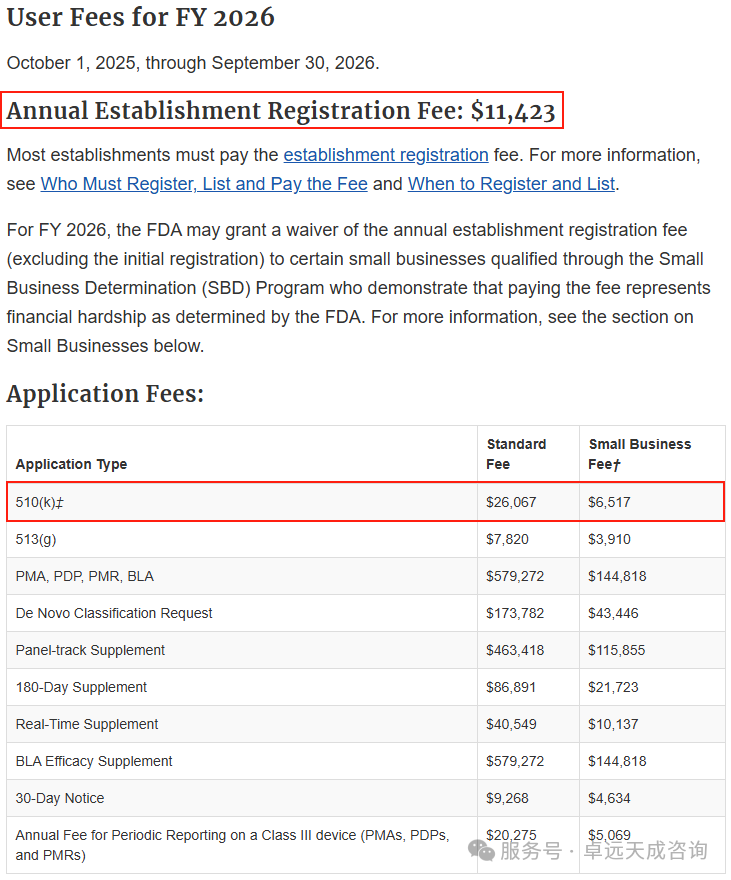
自2025年10月1日起至2026年9月30日,各项医疗器械的用户费用将有所调整。相比2025财年,各项费用有不同幅度的上涨,具体如下:(单位:美元)- 与2025财年(9280美元)对比,上涨23.1%。
- 2026财年FDA 510(k)评审费:26067美元。
- 与2025财年(24335美元)对比,上涨7.1%。
为确保各企业在2026财年继续处于有效的注册状态的同时兼顾费用的节省,在此做如下提醒:- 提前注册:2025年10月1日前有注册需求(如510K,PMA)的企业应加快资料递交的步伐,以享受2025财年的较低收费标准。
- 年费缴纳:自2025年10月1日起,企业即可开始缴纳FDA 2026财年的年费,并在2025年12月31日前完成企业年度注册更新。
- 避免延误:FDA网站在12月通常处于系统繁忙状态,请提前规划和准备,以免错过注册时间导致账户失效或被注销。
- 申请小企业资质:这是降低注册成本的重要途径。经FDA批准的小企业可享受用户费用75%的减免优惠,但FDA不对拥有小企业资格的企业实施年费减免。
* FDA小企业资格指的是公司(包括附属公司)最近税收年度的总收入或销售额未超过1亿美金。* FDA小企业资格不能跨越财政年度使用,如若需要请基于企业自身项目的申报进度计划安排小企业资格申报时间。小企业资格申请的官方审核时间为2个月。卓远天成 可为您提供美国小企业资格申请、美国代理人&企业注册服务,以及各个国家或地区医疗器械上市注册(如:美国FDA510K、欧盟CE认证、加拿大CMDCAS认证、澳洲TGA认证等)、医疗器械质量体系审查(如:美国QSR820验厂、中国医疗器械GMP(包括试剂类)、日本GMP、巴西GMP、ISO13485等)等多种国际注册及认证的咨询、代理服务;也可为您提供医疗器械风险管理、软件确认、灭菌确认、临床评估、可用性确认等专题培训服务,为您的产品上市&流通合规保驾护航。