

发布时间:2016-03-31
.jpg)
举办单位:

会议时间:2016年4月18日上午 10:00-12:30
会议地点:国家会展中心(上海) MI会议区 MI-03会议室
参与人员:医疗器械企业负责人、法规专员、注册专员、品质经理、技术管理者代表等
参会费用:每家公司2人免费(因场地有限,医疗器械生产企业优先)
会议摘要:
备受注目的医疗器械质量体系标准ISO 13485:2016已于3月1日正式发布。新版标准为医疗器械行业管理的法规化、医疗器械技术发展的国际化提供了更加良好的兼容性;同时也更加贴近企业实际,更具操作性。
那么,相对于旧版标准,新版标准具体有哪些显著变化呢?医疗器械企业应如何应对这些变化以适应医疗器械行业的发展趋势呢?卓远天成咨询将携手必维 国际检验集团为您全面解读。
The highly anticipated Medical device Quality System ISO 13485:2016 was already published in March 1st. This standard in new version
provides high compatibility for regularization of medical device industry management and internationalization of? medical device technology
development. Meanwhile, this standard draws closer to company's'reality and more operational. So, what are the obvious changes of the new
version when compares with the old one? And how will the medical device company deal with the changes in order to adapt to the developm-
ent trend of medical device. Shenzhen Joyantech Consulting Co., Ltd, together with Bureau Veritas, will comprehensively interpret this for you.
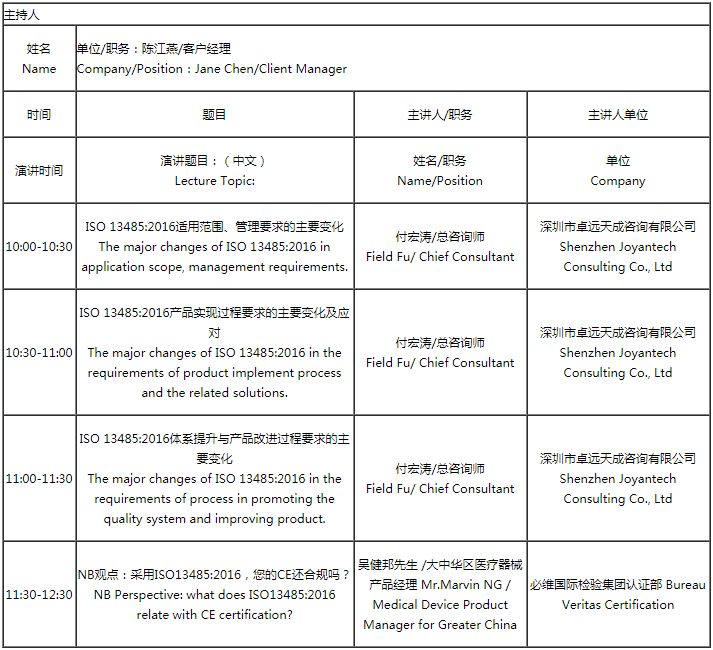
会议内容:


展会介绍: 中国国际医疗 器械博览会(CMEF),始创于1979年,每年春秋两届,在经历了30年的不断创新、自我完善,已成为亚太地区最大的 医疗器械及相关产品、 服务展览会。展出内容全面涵盖了包括医用影像、体外诊断、电子、光学、急救、康复护理以及医疗信息技术、外 包服务等上万种产品,直接并全面服务于医疗器械?行业从源头到终端整条医疗产业链。 每一届来自20 多个国家的2700余家 医疗器械生产企业和超过全球100多个国家和地区的150000人次的政府机构采购、医院买家和经 销商汇聚CMEF交易、交流;随着展览会更加专业化的纵深发展,先后创立了会议论坛、CMEF Imaging、CMEF IVD、CMEF IT、CMEF Orthopedics 以及ICMD一系列的医疗领域子品牌,CMEF已成为医疗行业内最大的专业医疗采购贸易平台、最佳的企业形象发布地以及专业 信息集散地和学术、技术交流平台。 卓远天成展位信息 深圳市卓远天成咨询公司介绍: 深圳市卓远天成咨询有限公司是一家从事医疗器械国际咨询的专业性咨询机构。提供各个国家或地区医疗器械上市注册(如:美国 FDA 510K、欧盟CE认证、加拿大CMDCAS认证、澳洲TGA认证等)、医疗器械质量体系审查(如:美国QSR820验厂、中国医疗器械GMP (包括试剂类)、日本GMP、巴西GMP、ISO13485等)等多种国际注册及认证的咨询、代理服务;也可为您提供医疗器械风险管理、软件 确认、灭菌确认、临床评估、可用性确认等专题培训服务。 卓远天成公司的咨询师及专家团队拥有大、中型医疗器械制造企业从事高级管理职位的工作经验及认证审核工作的专业背景,谙熟医 疗器械制造企业的运作模式和行业特点,精通欧盟、美国、加拿大、澳大利亚、日本、巴西及中国医疗器械法律法规、产品标准、技术规范, 在法规解读、标准理解、产品测试、文件编写、产品改进等方面具有较强的优势。 卓远天成公司与英、德、瑞士等国家的知名国际认证机构和国内权威认证机构和测试机构具有良好的合作关系。 报名注意事项: 请您下载附件,填写完整参会回执,并于04月15日前Email通知我们,我们将为您预留席位。 详情请联系:张小姐TEL:0755-86069197E-mail: info@cefda.com 关于卓远天成: 深圳市卓远天成咨询有限公司是一家从事医疗器械国际咨询的专业性咨询机构,可为您提供各个国家或地区医疗器械上市注册、医疗器 械质量体系审查等多种国际注册及认证的咨询/代理服务。

