

发布时间:2024-09-18
编者荐语:
卓远天成助力禾柏生物的糖化血红蛋白检测系统正式获得美国FDA批准!此为中国IVD行业首个通过FDA 510(k)认证的液相糖化血红蛋白测试系统(涵盖诊断与监测)。
以下文章来源于禾柏生物 ,作者禾柏生物
9月13日,禾柏生物的糖化血红蛋白检测系统正式获得美国FDA批准,成为中国IVD行业首个通过FDA 510(k) 认证的液相糖化血红蛋白测试系统(涵盖诊断与监测)。

糖化血红蛋白检测系统(包括糖化血红蛋白检测试剂盒及全自动免疫分析仪),作为禾柏生物的明星产品,自2019年起连续5年获得NGSP(National Glycohemoglobin Standardization Program,美国国家糖化血红蛋白标准化计划)认证。此次获得美国FDA 510(K)的注册认证,更是得到了全球最高标准的认可,为其在国际市场,尤其是美国市场的推广奠定了坚实的基础。
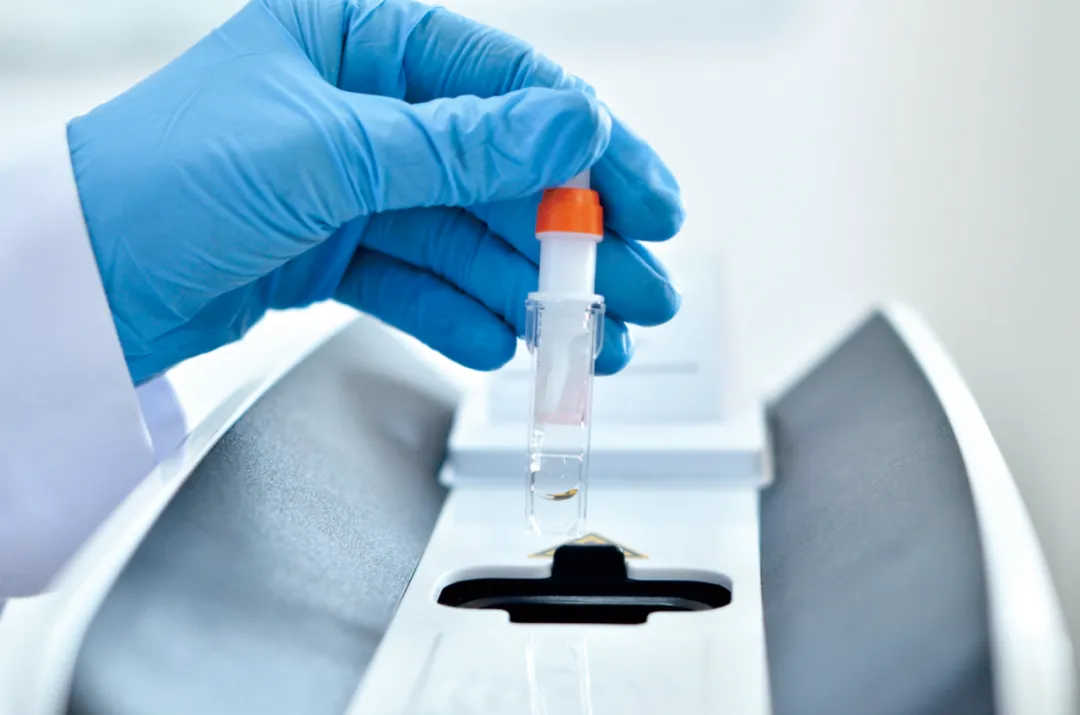
禾柏生物
糖化血红蛋白检测试剂盒和全自动免疫分析仪
国际顶尖的产品精准度
美国FDA,作为医药行业全球最具权威性的监管机构,以高难度著称,是各国公认的金牌认证。禾柏生物检测系统在认证过程中通过了产品分析性能验证、临床评价、运输验证等一系列考验,历时3年,多次交互审核,并在中国唯一一家NGSP II级参考实验室---上海复旦大学附属中山医院,进行了全方位的临床测试。禾柏生物糖化血红蛋白检测系统与伯乐HPLC糖化血红蛋白检测系统进行对比,相关性和一致性均有良好的表现:
禾柏生物检测系统和伯乐检测系统的检测结果相关系数(r)为0.9972,满足FDA r≥0.975的要求,表明两种系统的检测结果有非常高的相关性。回归方程:y = 1.0089x-0.0727,斜率1.0089 (0.9952,1.0226),截距-0.0727 (-0.1775,0.0321),满足斜率接近1截距接近0的要求,说明两种试剂有高度的一致性。(详见下图)
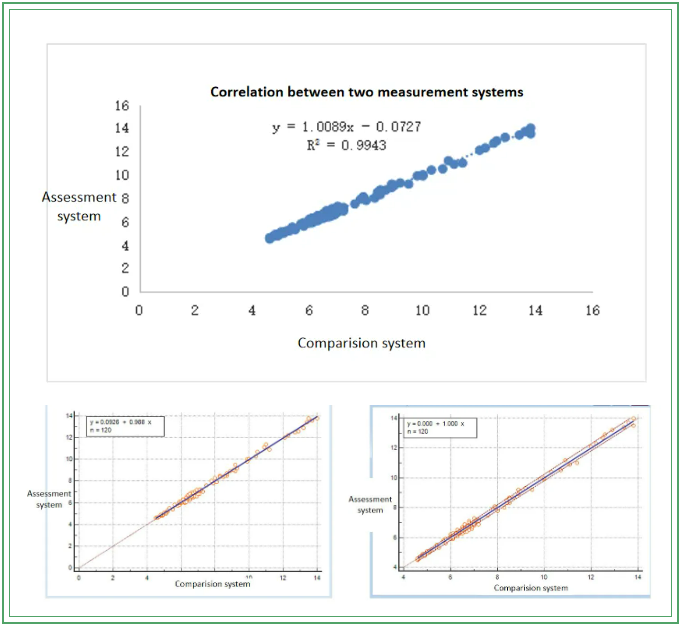
禾柏国际市场一路高歌
FDA认证,不仅是进入美国市场的一张门票,更是在全球打开一扇信任的窗。在许多国家和地区,FDA认证是产品进入市场的必要条件或加分项,获得FDA认证可以大大简化产品进入这些市场的程序,这对已经成功开发104个国家的禾柏国际市场无疑是重大利好,助力销售业绩突飞猛进。
对于禾柏生物来说,获得FDA认证不仅是对其现有产品质量的肯定,也是对技术创新能力和市场开拓能力的认可。未来,随着国际市场影响力的不断提升,禾柏生物将吸引更多的合作伙伴和客户,为公司的全球化发展注入新的活力。